******医院******管理局综合和规划财务司和国家卫生健康委办公厅联合发布的《关于开展******医院自行研制体外诊断试剂委托生产企业的情况进行公开市场调研,欢迎符合条件并有合作意向的企业积极报名参与。
一、调研期限
1.1、自公告发布之日起5个工作日内,逾期不予受理。
二、涉及试剂生产需求
2.1、项目编号:2025-DY-003
2.2、实体瘤1021基因突变检测
2.3、调研列表范围:

三、报名生产企业须符合条件
3.1、具备医疗器械生产许可证且住所及生产地址为北京;
3.2、提供医疗器械生产许可证,明确生产范围覆盖IVD相关类别,需涵盖三类体外诊断试剂;
3.3、投标企业需通过国家药监局(NMPA)的GMP认证,并具备有效期内认证证书;
3.4、质量管理体系按照ISO13485《医疗器械质量管理体系用于法规的要求》运行;
3.5、生产、质量、技术负责人需具备相关专业背景(如生物医学、检验学)及3年以上行业经验;
3.6、生产环境要求:十万级洁净区、十万级洁净区+生物安全柜、万级洁净区、万级洁净区+生物安全柜;半成品中间品保存环境(-20℃±5℃、2`8℃);
3.7、设备要求:需具备配制、退货、离心、震荡混匀、打断、分装等工序需求设备;
3.8、人员要求:须具备有资质生产人员;
3.9、工艺要求:相关工艺文件齐全,能够指导人员操作,生产工艺流程按甲方要求进行生产;
3.10、检验项目:复核COA、外观、PH、酶的功能性、含量、浓度、片段大小-琼脂糖电泳等操作;
3.11、质控条件:要求供应商对每个产品制定单独的产品工艺规程,对物料及产品质量标准进行了明确规定,产品质量标准符合产品技术要求,确保产品在可控的生产条件下进行生产,生产过程严格按照生产工艺规程进行,保证产品检测结果的准确性,所有的原辅料、包材等均需检测放行后,方可进行下一工序操作。
3.12、供应商******医院和药监部门核查,提供质量管理方案。
3.13、生产周期及产品供应条件:生产周期小于20个自然日,收到订单后20个自然日内发货。
四、报名企业提供资料
1.企业营业执照;
2.医疗器械生产许可证;
3.生产质量体系证书;
4.调研信息表(见附件)。
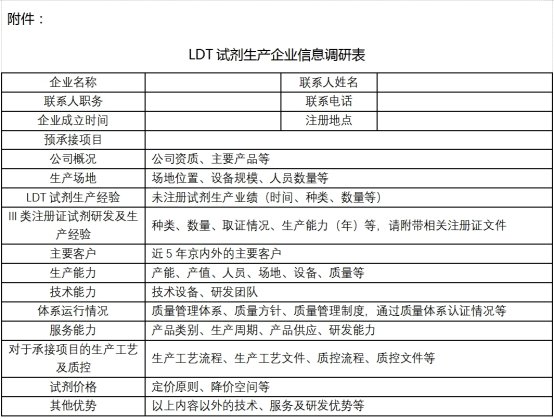
五、报名方法
请将上述资料须加盖公章,扫描件电子版发送至邮箱:******
联系人:焉老师
电话:******
【1】凡本网注明来源:"今日招标网"的所有文字、图片和音视频稿件,版权均属于今日招标网,转载请必须注明机今日招标网,违反者本网将追究相关法律责任。
【2】本网转载并注明自其它来源的作品,是本着为读者传递更多信息之目的,并不代表本网赞同其观点或证实其内容的真实性,不承担此类作品侵权行为的直接责任及连带责任。其他媒体、网站或个人从本网转载时,必须保留本网注明的作品来源,并自负版权等法律责任。
【3】如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系。









